| Използвайки Economy.bg, Вие се съгласявате с "Политика за Cookies/Бисквитки" , необходими за пълната функционалност на услугата. [X] |
|
1218 прочитания
ЕМА започва оценка на ваксината на Pfizer за тийнейджъри
В САЩ предстои одобряването ѝ за деца от 12 до 15 години до седмица
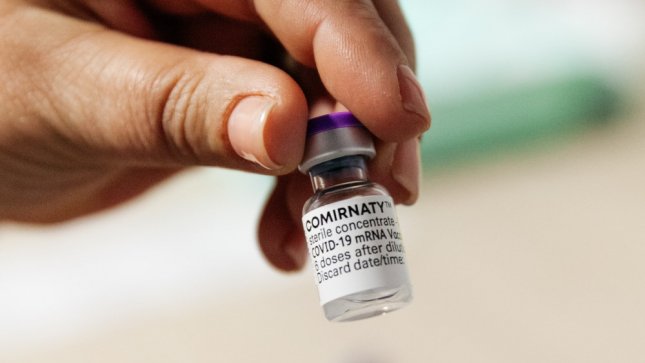 Европейската агенция по лекарствата (EMA) обяви, че е започнала оценка на искане от Pfizer/BioNTech за разширяване на употребата на ваксината им срещу Covid-19 за млади хора на възраст от 12 до 15 години. Ходът идва на фона на съобщения, че американският надзорен орган ще разреши използването му за младежи до следващата седмица. „Комитетът на EMA за хуманни лекарства (CHMP) ще извърши ускорена оценка на данните, представени от компанията, която предлага на пазара Comirnaty, включително резултати от голямо текущо клинично проучване, включващо юноши на възраст над 12 години, за да реши дали да препоръча удължаването на индикация“, се посочва в декларация на агенцията. Резултатът от тяхната оценка се очаква да бъде обявен през юни. В заявлението си до EMA, подадено на 30 април, Pfizer и BioNtech заявяват, че данните от фаза 3 на клинично изпитване, включващо 2260 американски участници на възраст от 12 до 15 години „показват ефективност на ваксината от 100% при участници със или без предварително SARS-CoV- 2 инфекция и силни имунни отговори с антитела.“ Те добавят, че ваксината също се понася добре, като страничните ефекти са подобни на наблюдаваните при възрастни хора. Те включват болка на мястото на инжектиране, умора, треска, главоболие и студени тръпки. Междувременно Американската администрация по храните и лекарствата (FDA) може да даде разрешение до началото на следващата седмица и дори по-рано, заяви федерален служител, който говори пред агенция AP без да бъде назоваван. Това може да даде възможност за ваксинация на младежи преди началото на следващата учебна година. Ваксината на Pfizer/BioNTech, известна още като Comirnaty, вече е разрешена за употреба на хора на възраст 16 и повече години в САЩ и Европейския съюз. Лицето, запознато с процеса, което говори под условие за анонимност, за да сподели вътрешни въпроси, потвърди хронологията и добави, че се очаква FDA да одобри използването на Pfizer от дори по-малки деца някъде тази есен. Pfizer не е единствената компания, която се стреми да намали възрастовата граница за своята ваксина. Очакват се резултати и до средата на тази година от американско проучване на ваксината на Moderna при 12 до 17-годишни. Но в знак, че констатациите са обещаващи, FDA вече е позволила на двете компании да започнат американски проучвания при деца на 11 и по-малко години, като проправят пътя към 6-месечна възраст. Повечето ваксини срещу Covid-19, одобрени от властите по света, са за възрастни, които са изложени на по-висок риск, но здравните служители смятат, че ваксинирането на деца от всички възрасти ще бъде от решаващо значение за спирането на пандемията. Някои изследвания показват, че по-големите деца могат да играят роля в разпространението на вируса, припомня Euronews.
|
Искам да се абонирам за седмичния бюлетин на Economy.bg:
* Въведеният имейл се използва само за целите на абонамента, имате възможност да прекратите абонамента по всяко време.
|
|
|
|
Copyright © 2024 economy.bg. Издание
на jobs.bg
|